Química Orgânica II
Lista de 30 exercícios de Química com gabarito sobre o tema Química Orgânica II com questões do Enem.
Você pode conferir as videoaulas, conteúdo de teoria, e mais questões sobre o tema Química Orgânica II.
01. (Enem PPL 2020) O propranolol é um fármaco pouco solúvel em água utilizado no tratamento de algumas doenças cardiovasculares. Quando essa substância é tratada com uma quantidade estequiométrica de um ácido de Brönsted-Lowry, o grupamento de maior basicidade reage com o próton levando à formação de um derivado solúvel em água.

O ácido de Brönsted-Lowry reage com
- a hidroxila alcoólica.
- os anéis aromáticos.
- as metilas terminais.
- o grupamento amina.
- o oxigênio do grupamento éter.
02. (Enem PPL 2020) A pentano-5-lactama é uma amida cíclica que tem aplicações na síntese de fármacos e pode ser obtida pela desidratação intramolecular, entre os grupos funcionais de ácido carboxílico e amina primária, provenientes de um composto de cadeia alifática, saturada, normal e homogênea.

O composto que, em condições apropriadas, dá origem a essa amida cíclica é
- CH₃NHCH₂CH₂CH₂CO₂H.
- HOCH = CHCH₂CH₂CONH₂.
- CH₂(NH₂)CH₂CH = CHCO₂H.
- CH₂(NH₂)CH₂CH₂CH₂CO₂H.
- CH₂(NH₂)CH(CH₃)CH₂CO₂H.
03. (Enem 2019) Glicólise é um processo que ocorre nas células, convertendo glicose em piruvato. Durante a prática de exercícios físicos que demandam grande quantidade de esforço, a glicose é completamente oxidada na presença de O2. Entretanto, em alguns casos, as células musculares podem sofrer um déficit de O2 e a glicose ser convertida em duas moléculas de ácido lático. As equações termoquímicas para a combustão dá glicose e do ácido lático são, respectivamente, mostradas a seguir:
C6H12O6 (s) + 6 O2 (g) → 6 CO2 (g) + 6 H2O (l) ΔCH = - 2800kJ
CH3CH(OH)COOH (s) + 3 O2 (g) → 3 CO2 (g) + 3 H2O (l) ΔCH = - 1 344kJ
O processo anaeróbico é menos vantajoso energeticamente porque
- libera 112 kJ por mol de glicose.
- libera 467 kJ por mol de glicose.
- libera 2 688 kJ por mol de glicose.
- absorve 1 344 kJ por mol de glicose.
- absorve 2 800 kJ por mol de glicose.
04. (Enem 2019) Os hidrocarbonetos são moléculas orgânicas com uma série de aplicações industriais. Por exemplo, eles estão presentes em grande quantidade nas diversas frações do petróleo e normalmente são separados por destilação fracionada, com base em suas temperaturas de ebulição. O quadro apresenta as principais frações obtidas na destilação do petróleo em diferentes faixas de temperaturas.

Na fração 4, a separação dos compostos ocorre em temperaturas mais elevadas porque
- suas densidades são maiores.
- o número de ramificações é maior.
- sua solubilidade no petróleo é maior.
- as forças intermoleculares são mais intensas.
- a cadeia carbônica é mais difícil de ser quebrada.
05. (Enem 2019) O odor que permanece nas mãos após o contato com alho pode ser eliminado pela utilização de um “sabonete de aço inoxidável”, constituído de aço inox (74%), cromo e níquel. A principal vantagem desse “sabonete” é que ele não se desgasta com o uso. Considere que a principal substância responsável pelo odor de alho é a alicina (estrutura I) e que, para que o odor seja eliminado, ela seja transformada na estrutura II.

Na conversão de I em II, o “sabonete” atuará como um
- ácido.
- redutor.
- eletrólito.
- tensoativo.
- catalisador.
06. (Enem 2019) Uma das técnicas de reciclagem química do polímero PET [poli(tereftalato de etileno)] gera o tereftalato de metila e o etanodiol, conforme o esquema de reação, e ocorre por meio de uma reação de transesterificação.

O composto A, representado no esquema de reação, é o
- metano.
- metanol.
- éter metílico.
- ácido etanoico.
- anidrido etanoico.
07. (Enem 2018) Tensoativos são compostos orgânicos que possuem comportamento anfifílico, isto é, possuem duas regiões, uma hidrofóbica e outra hidrofílica. O principal tensoativo aniônico sintético surgiu na década de 1940 e teve grande aceitação no mercado de detergentes em razão do melhor desempenho comparado ao do sabão. No entanto, o uso desse produto provocou grandes problemas ambientais, dentre eles a resistência à degradação biológica, por causa dos diversos carbonos terciários na cadeia que compõe a porção hidrofóbica desse tensoativo aniônico. As ramificações na cadeia dificultam sua degradação, levando à persistência no meio ambiente por longos períodos. Isso levou a sua substituição na maioria dos países por tensoativos biodegradáveis, ou seja, com cadeias alquílicas lineares.
PENTEADO, J. C. P.; EL SEOUD, O. A.; CARVALHO, L. R. F. [ ... ]: uma abordagem ambiental e analítica. Química Nova, n. 5, 2006 (adaptado).
Qual a fórmula estrutural do tensoativo persistente no ambiente mencionado no texto?
08. (Enem 2018) Pesquisas demonstram que nanodispositivos baseados em movimentos de dimensões atômicas, induzidos por luz, poderão ter aplicações em tecnologias futuras, substituindo micromotores, sem a necessidade de componentes mecânicos. Exemplo de movimento molecular induzido pela luz pode ser observado pela flexão de uma lâmina delgada de silício, ligado a um polímero de azobenzeno e a um material suporte, em dois comprimentos de onda, conforme ilustrado na figura. Com a aplicação de luz ocorrem reações reversíveis da cadeia do polímero, que promovem o movimento observado.
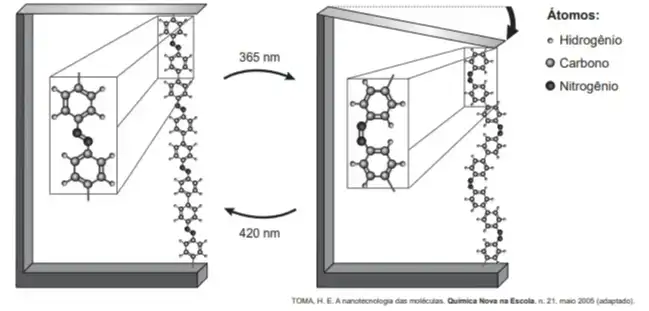
O fenômeno de movimento molecular, promovido pela incidência de luz, decorre do(a)
- movimento vibracional dos átomos, que leva ao encurtamento e à relaxação das ligações.
- isomerização das ligações N = N, sendo a forma cis do polímero mais compacta que a trans.
- tautomerização das unidades monoméricas do polímero, que leva a um composto mais compacto.
- ressonância entre os elétrons π do grupo azo e os do anel aromático que encurta as ligações duplas.
- variação conformacional das ligações N = N, que resulta em estruturas com diferentes áreas de superfície.
09. (Enem 2018) As abelhas utilizam a sinalização química para distinguir a abelha-rainha de uma operária, sendo capazes de reconhecer diferenças entre moléculas. A rainha produz o sinalizador químico conhecido como ácido 9-hidroxidec-2-enoico, enquanto as abelhas-operárias produzem ácido 10-hidroxidec-2-enoico. Nós podemos distinguir as abelhas-operárias e rainhas por sua aparência, mas, entre si, elas usam essa sinalização química para perceber a diferença. Pode-se dizer que veem por meio da química.
LE COUTEUR, P.; BURRESON, J. Os botões de Napoleão: as 17 moléculas que mudaram a história. Rio de Janeiro: Jorge Zahar, 2006 (adaptado).
As moléculas dos sinalizadores químicos produzidas pelas abelhas rainha e operária possuem diferença na
- fórmula estrutural.
- fórmula molecular.
- identificação dos tipos de ligação.
- contagem do número de carbonos.
- identificação dos grupos funcionais.
10. (Enem 2018) O petróleo é uma fonte de energia de baixo custo e de larga utilização como matéria-prima para uma grande variedade de produtos. É um óleo formado de várias substâncias de origem orgânica, em sua maioria hidrocarbonetos de diferentes massas molares. São utilizadas técnicas de separação para obtenção dos componentes comercializáveis do petróleo.
Além disso, para aumentar a quantidade de frações comercializáveis, otimizando o produto de origem fóssil, utiliza-se o processo de craqueamento.
O que ocorre nesse processo?
- Transformação das frações do petróleo em outras moléculas menores.
- Reação de óxido-redução com transferência de elétrons entre as moléculas.
- Solubilização das frações do petróleo com a utilização de diferentes solventes.
- Decantação das moléculas com diferentes massas molares pelo uso de centrífugas.
- Separação dos diferentes componentes do petróleo em função de suas temperaturas de ebulição.
11. (Enem 2018) A hidroxilamina (NH2OH) é extremamente reativa em reações de substituição nucleofílica, justificando sua utilização em diversos processos. A reação de substituição nucleofílica entre o anidrido acético e a hidroxilamina está representada.

O produto A é favorecido em relação ao B, por um fator de 105. Em um estudo de possível substituição do uso de hidroxilamina, foram testadas as moléculas numeradas de 1 a 5.

Dentre as moléculas testadas, qual delas apresentou menor reatividade?
- 1
- 2
- 3
- 4
- 5
12. (Enem 2018) O grafeno é uma forma alotrópica do carbono constituído por uma folha planar (arranjo bidimensional) de átomos de carbono compactados e com a espessura de apenas um átomo. Sua estrutura é hexagonal, conforme a figura.

Nesse arranjo, os átomos de carbono possuem hibridação
- sp de geometria linear.
- sp2de geometria trigonal planar.
- sp3alternados com carbonos com hibridação sp de geometria linear.
- sp3d de geometria planar.
- sp3d2 com geometria hexagonal planar.
13. (Enem 2017) A ozonólise, reação utilizada na indústria madeireira para a produção de papel, é também utilizada em escala de laboratório na síntese de aldeídos e cetonas. As duplas ligações dos alcenos são clivadas pela oxidação com o ozônio (03), em presença de água e zinco metálico, e a reação produz aldeídos e/ou cetonas, dependendo do grau de substituição da ligação dupla. Ligações duplas dissubstituídas geram cetonas, enquanto as ligações duplas terminais ou monossubstituídas dão origem a aldeídos, como mostra o esquema.

Considere a ozonólise do composto 1-fenil-2-metilprop-1-eno:
Quais são os produtos formados nessa reação?

- Benzaldeído e propanona.
- Propanal e benzaldeído.
- 2-fenil-etanal e metanal.
- Benzeno e propanona.
- Benzaldeído e etanal.
14. (Enem 2017) O biodiesel é um biocombustível obtido a partir de fontes renováveis, que surgiu como alternativa ao uso do diesel de petróleo para motores de combustão interna. Ele pode ser obtido pela reação entre triglicerídeos, presentes em óleos vegetais e gorduras animais, entre outros, e álcoois de baixa massa molar, como o metanol ou etanol, na presença de um catalisador, de acordo com a equação química:

A função química presente no produto que representa o biodiesel é
- éter.
- éster.
- álcool.
- cetona.
- acido carboxílico.
15. (Enem 2017) O ácido acetilsalicílico, AAS (massa molar igual a 180 g/mol), é sintetizado a partir da reação do ácido salicílico (massa molar igual a 138 g/mol) com anidrido acético, usando-se ácido sulfúrico como catalisador, conforme a equação química:

Após a síntese, o AAS é purificado e o rendimento flnal é de aproximadamente 50%. Devido às suas propriedades farmacológicas (antitérmico, analgésico, anti-inflamatório e antitrombótico), o AAS é utilizado como medicamento na forma de comprimidos, nos quais se emprega tipicamente uma massa de 500 mg dessa substância.
Uma indústria farmacêutica pretende fabricar um lote de 900 mil comprimidos, de acordo com as especificações do texto.
Qual é a massa de ácido salicílico, em kg, que deve ser empregada para esse fim?
- 293
- 345
- 414
- 690
- 828
16. (Enem PPL 2017) O hidrocarboneto representado pela estrutura química a seguir pode ser isolado e partir das folhas ou das flores de determinadas plantas. Além disso, sua função é relacionada, entre outros fatores, a seu perfil de insaturações.

Considerando esse perfil específico, quantas ligações pi a molécula contém?
- 1
- 2
- 4
- 6
- 7
17. (Enem PPL 2017) Em algumas regiões brasileiras, é comum se encontrar um animal com odor característico, o zorriIho. Esse odor serve para a proteção desse animal, afastando seus predadores. Um dos feromônios responsáveis por esse odor é uma substância que apresenta isomeria trans e um grupo tioI ligado à sua cadeia.
A estrutura desse feromônio, que ajuda na proteção do zorriIho, é
18. (Enem PPL 2017) Os polímeros são materiais amplamente utilizados na sociedade moderna, alguns deles na fabricação de embalagens e filmes plásticos, por exemplo. Na figura estão relacionadas as estruturas de alguns monômeros usados na produção de polímeros de adição comuns.

Dentre os homopolímeros formados a partir dos monômeros da figura, aquele que apresenta solubilidade em água é
- polietileno.
- poliestireno.
- polipropileno.
- poliacrilamida.
- policloreto de vinila.
19. (Enem 2016) O esquema representa, de maneira simplificada, o processo de produção de etanol utilizando milho como matéria-prima.

A etapa de hidrólise na produção de etanol a partir do milho é fundamental para que
- a glicose seja convertida em sacarose.
- as enzimas dessa planta sejam ativadas.
- a maceração favoreça a solubilização em água.
- o amido seja transformado em substratos utilizáveis pela levedura.
- os grãos com diferentes composições químicas sejam padronizados.
20. (Enem 2016) Os feromônios são substâncias utilizadas na comunicação entre indivíduos de uma espécie. O primeiro feromônio isolado de um inseto foi o bombicol, substância produzida pela mariposa do bicho-da-seda.
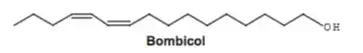
O uso de feromônios em ações de controle de insetos-praga está de acordo com o modelo preconizado para a agricultura do futuro. São agentes altamente específicos e seus compostos químicos podem ser empregados em determinados cultivos, conforme ilustrado no quadro.
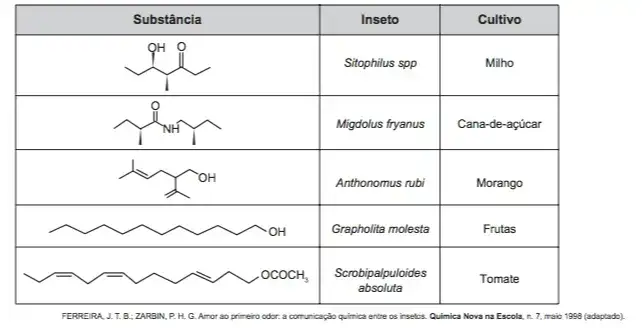
Considerando essas estruturas químicas, o tipo de estereoisomeria apresentada pelo bombicol é também apresentada pelo feromônio utilizado no controle do inseto
- Sitophilus spp.
- Migdolus fryanus.
- Anthonomus rubi.
- Grapholita molesta.
- Scrobipalpuloides absoluta.
21. (Enem 2016) Em sua formulação, o spray de pimenta contém porcentagens variadas de oleorresina de Capsicum, cujo princípio ativo é a capsaicina, e um solvente (um álcool como etanol ou isopropanol). Em contato com os olhos, pele ou vias respiratórias, a capsaicina causa um efeito inflamatório que gera uma sensação dor e ardor, levando à cegueira temporária. O processo é desencadeado pela liberação de neuropeptídios das terminações nervosas.
Disponível em: http://pessoas.hsw.uol.com.br. Acesso em: 1 mar. 2012 (adaptado).
Quando uma pessoa é atingida com o spray de pimenta nos olhos ou na pele, a lavagem da região atingida com água é ineficaz porque a
- reação entre o etanol e água libera calor, intensificado o ardor.
- solubilidade do princípio ativo em água é muito baixa, dificultando a sua remoção.
- permeabilidade da água na pele é muito alta, nãopermitindo a remoção do princípio ativo.
- solubilização do óleo em água causa um maior espalhamento além das áreas atingidas.
- ardência faz evaporar rapidamente a água, não permitindo que haja contato entre o óleo e o solvente.
22. (Enem 2016) Nucleófilos (Nu-) são bases de Lewis que reagem com haletos de alquila, por meio de uma reação chamada substituição nucleofílica (SN), como mostrado no esquema:
R - X + Nu- → R - Nu + X-
(R = grupo alquila e X = halogênio)
A reação de SN entre metóxido de sódio (Nu- = CH3O-) e brometo de metila fornece um composto orgânico pertencente à função
- éter.
- éster.
- álcool.
- haleto.
- hidrocarboneto.
23. (Enem 2016) A lipofilia é um dos fatores fundamentais para o planejamento de um fármaco. Ela mede o grau de afinidade que a substância tem com ambientes apolares, podendo ser avaliada por seu coeficiente de participação.
Em relação ao coeficiente de participação da testosterona, as lipofilias dos compostos 1 e 2 são, respectivamentes,

- menor e menor que a lipofilia da testosterona.
- menor e maior que a lipofilia da testosterona.
- maior e menor que lipofilia da testosterona.
- maior e maior que a lipofilia da testosterona.
- menor e igual à lipofilia da testosterona.
24. (Enem PPL 2016) As sacolas plásticas são utilizadas em grande quantidade no Brasil por serem práticas, leves e de baixo custo. Porém, o tempo necessário para que sofram degradação nas condições do meio é de, no mínimo, 100 anos. Com o intuito de reduzir o impacto ambiental desses produtos, as sacolas biodegradáveis foram introduzidas no mercado. Essas sacolas são confeccionadas de um material polimérico que confere a elas uma característica que as torna biodegradáveis.
A qual característica das sacolas biodegradáveis o texto faz referência?
- Elevada massa molecular do polímero.
- Espessura fina do material que as constitui.
- Baixa resistência aos líquidos nas condições de uso.
- Baixa resistência ao ataque por microrganismos em condições adequadas.
- Ausência de anéis aromáticos na estrutura do polímero usado na confecção das sacolas.
25. (Enem PPL 2016) Algumas práticas agrícolas fazem uso de queimadas, apesar de produzirem grandes efeitos negativos. Por exemplo, quando ocorre a queima da palha de cana-de-açúcar, utilizada na produção de etanol, há emissão de poluentes como CO2, SOx, NOx e materiais particulados (MP) para a atmosfera. Assim, a produção de biocombustíveis pode, muitas vezes, ser acompanhada da emissão de vários poluentes.
CARDOSO, A. A.; MACHADO, C. M. D.; PEREIRA, E. A. Biocombustível: o mito do combustível limpo. Química Nova na Escola, n. 28, maio 2008 (adaptado).
Considerando a obtenção e o consumo desse biocombustível, há transformação química quando
- o etanol é armazenado em tanques de aço inoxidável.
- a palha de cana-de-açúcar é exposta ao sol para secagem.
- a palha da cana e o etanol são usados como fonte de energia.
- os poluentes SOx, NOx e MP são mantidos intactos e dispersos na atmosfera.
- os materiais particulados (MP) são espalhados no ar e sofrem deposição seca.
26. (Enem PPL 2016) O petróleo é um tipo de combustível fóssil, de origem animal e vegetal, constituído principalmente por hidrocarbonetos. Em desastres de derramamento de petróleo, vários métodos são usados para a limpeza das áreas afetadas. Um deles é a biodegradação por populações naturais de microrganismos que utilizam o petróleo como fonte de nutrientes. O quadro mostra a composição química média das células desses microrganismos.

Para uma efetiva biodegradação, a região afetada deve ser suplementada com
- nitrogênio e fósforo.
- hidrogênio e fósforo.
- carbono e nitrogênio.
- carbono e hidrogênio.
- nitrogênio e hidrogênio.
27. (Enem PPL 2016) A descoberta dos organismos extremófilos foi uma surpresa para os pesquisadores. Alguns desses organismos, chamados de acidófilos, são capazes de sobreviver em ambientes extremamente ácidos. Uma característica desses organismos é a capacidade de produzir membranas celulares compostas de lipídeos feitos de éteres em vez dos ésteres de glicerol, comuns nos outros seres vivos (mesófilos), o que preserva a membrana celular desses organismos mesmo em condições extremas de acidez.
A degradação das membranas celulares de organismos não extremófilos em meio ácido é classificado como
- hidrólise.
- termólise.
- eterificação
- condensação.
- saponificação
28. (Enem 2016 - 3.ª Aplicação) O quadro apresenta alguns exemplos de combustíveis empregados em residências, indústrias e meios de transporte.

São combustíveis líquidos à temperatura ambiente de 25 ºC:
- Butano, etanol e metano.
- Etanol, metanol e octano.
- Metano, metanol e octano.
- Metanol e metano.
- Octano e butano.
29. (Enem 2016 - 3.ª Aplicação) A busca por substâncias capazes de minimizar a ação do inseto que ataca as plantações de tomate no Brasil levou à síntase e ao emprego de um feromônio sexual com a seguinte fórmula estrutural:

Uma indústria agroquímica necessita sintetizar um derivado com maior eficácia. Para tanto, o potencial substituto deverá preservar as seguintes propriedades estruturais do feromônio sexual: função orgânica, cadeia normal e a isomeria geométrica original.
A fórmula estrutural do substituto adequado ao feromônio sexual obtido industrialmente é:
30. (Enem 2015) Uma forma de organização de um sistema biológico é a presença de sinais diversos utilizados pelos indivíduos para se comunicarem. No caso das abelhas da espécie Apis mellifera, os sinais utilizados podem ser feromônios. Para saírem e voltarem de suas colmeias, usam um feromônio que indica a trilha percorrida por elas (Composto A). Quando pressentem o perigo, expelem um feromônio de alarme (Composto B), que serve de sinal para um combate coletivo. O que diferencia cada um desses sinais utilizados pelas abelhas são as estruturas e funções orgânicas dos feromônios.

As funções orgânicas que caracterizam os feromônios de trilha e de alarme são, respectivamente,
- álcool e éster.
- aldeído e cetona.
- éter e hidrocarboneto.
- enol e ácido carboxílico.
- ácido carboxílico e amida.














