Distribuição ou Configuração Eletrônica
Níveis e Subníveis
Os níveis são representados por números de 1 a 7, e são equivalentes às camadas (K, L, M, N, O, P e Q).
Tabelas dos Níveis e Subníveis de Energia
| Níveis | Camada | Nº Máximo de Elétrons | Valor do Subnível |
|---|---|---|---|
| 2 6 10 14 | |||
| n = 1 | K | 2 | 1s |
| n = 2 | L | 8 | 2s 2p |
| n = 3 | M | 18 | 3s 3p 3d |
| n = 4 | N | 32 | 4s 4p 4d 4f |
| n = 5 | O | 32 | 5s 5p 5d 5f |
| n = 6 | P | 18 | 6s 6p 6d |
| n = 7 | Q | 8 | 7s 7p 7d |
Diagrama de Pauling
O Diagrama de Pauling é uma representação gráfica que facilita a visualização da ordem crescente de energia dos subníveis.
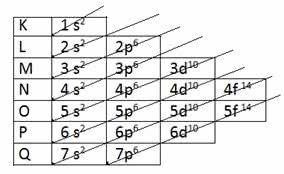
O Diagrama de Pauling é lido na diagonal começando por:
1s < 2s < 2p < 3s < 3p < 4s < 3d < 4p < 5s < 4d < 5p < 6s < 4f < 5d < 6p < 7s < 5f < 6d <7p
| Valor máximo de elétrons em cada subnível |
|---|
| s = 2 |
| p = 6 |
| d = 10 |
| f = 14 |
Distribuição eletrônica na prática

Qual a distribuição eletrônica do 4Be?
Ao observar o Diagrama de Pauling notamos que sempre existe um número máximo de elétrons, então sabemos o valor do Berílio, precisamos chegar ao valor 4, que é o seu número atômico.
4Be = 1S2 2S2
O valor máximo do 1S é 2, e do 2S é 2, logo o resultado é 4.
Agora vamos fazer um exemplo mais longo
Qual a distribuição eletrônica do 38Sr?
38Sr = 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2
Note que a soma dos elétrons deu 38.
Lembre-se: O Diagrama de Pauling segue em vertical, então só vá para a próxima após o término da primeira.
Camada de Valência:
A camada de valência (CV) é o último nível de uma distribuição eletrônica.
No 4Be a camada de valência é a segunda camada, uma vez que ela é a que está mais longe.
No 38Sr (estrôncio) a Camada de valência é a quinta camada, devido o 5s2 está último nível em relação aos demais.

Cristais de estrôncio (Sr) (Wikimedia Commons/Alchemist-hp)
Dica: No dois exemplos acima a camada de valencia está relacionada com ultimo valor, porém isso não é uma regra.
Subnivel Mais Energetico:
O subnivel mais energético é o ultimo valor da nossa distribuicao:
No 4Be 2s2 (dois elétrons) e no 38Sr 2s2 (dois elétrons).
Qual a distribuição eletrônica do 23Fe+3?
Note que agora existe uma nova situação, um íon +3 no Ferro. Como proceder?
Primeiramente vamos fazer a distribuição eletrônica normalmente.
23Fe = 1s2 2s2 2p6 3s2 3p6 4s2 3d6
Como o ferro tem o ion de +3, nós vamos retirar 3 elétrons, sendo que primeiro vamos retirar da camada de valência que é o 4s2.
23Fe+3 = 1s2 2s2 2p6 3s2 3p6 3d6
Note que retiramos dois átomos, porém falta mais um. Ele será retirado do subnível mais energético que é o último valor.
23Fe+3 = 1s2 2s2 2p6 3s2 3p6 3d5
Exemplos de distribuição de elétrons na eletrosfera
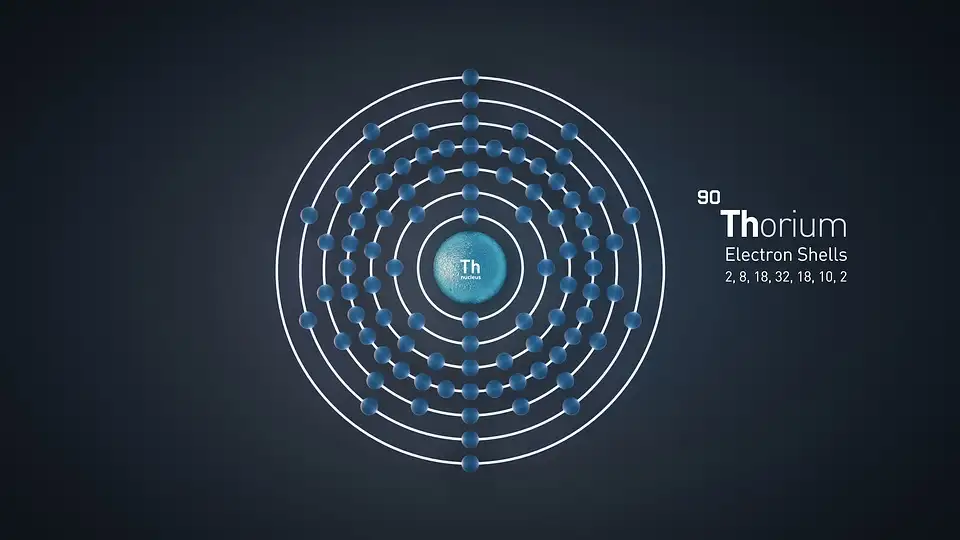
Distribuição eletrônica do Tório, que foi descoberto em 1828 por Jöns Jacob Berzelius. O seu nome é em homenagem a Thor, deus escandinavo do trovão.
| Elemento | Número Atômico | Distribuição eletrônica | |
|---|---|---|---|
| He | Z = 2 | 1s2 | |
| L | Z = 3 | 1s2 2s1 | |
| Be | Z = 4 | 1s2 2s2 | |
| B | Z = 5 | 1s2 2s2 2p1 | |
| C | Z = 6 | 1s2 2s2 2p2 | |
| N | Z = 7 | 1s2 2s2 2p3 | |
| O | Z = 8 | 1s2 2s2 2p4 | |
| F | Z = 9 | 1s2 2s2 2p5 | |
| Ne | Z = 10 | 1s2 2s2 2p6 | |
| Na | Z = 11 | 1s2 2s2 2p6 3s1 |
Tabela Periódica

A Tabela periódica apresenta o número atômico de todos os elementos, sendo o hidrogênio 1 e o oganessono 118.
Lista Geral de Questões
Referências:
USBERCO, João; SALVADOR, Edgard. Conecte Química. São Paulo: Saraiva S.A, 2014.